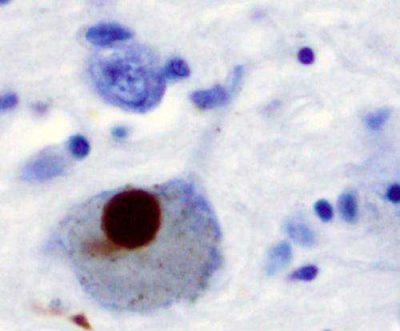
(Parkinson-immagine: immunoistochimica per alfa-sinucleina che mostra una colorazione positiva (marrone) di un corpo di Lewy intraneurale nella Substantia nigra nella malattia di Parkinson. Credito: Wikipedia).
In una scoperta inaspettata, i ricercatori del Georgetown University Medical Center hanno identificato quello che sembra essere un difetto vascolare significativo nei pazienti con malattia di Parkinson moderatamente grave. La scoperta potrebbe aiutare a spiegare un risultato precedente dello stesso studio, in cui il farmaco Nilotinib è stato in grado di arrestare il declino motorio e non motorio (cognizione e qualità della vita) a lungo termine.
I ricercatori affermano che la loro scoperta, dettagliata in uno studio pubblicato il 12 novembre 2021, su Neurology Genetics, suggerisce che le pareti dei vasi sanguigni chiamate barriera ematoencefalica che normalmente agiscono come un filtro cruciale per proteggere il cervello dalle tossine e per consentire il passaggio di nutrienti per nutrirlo, non funzionano correttamente in alcuni pazienti di Parkinson: impedisce alle tossine di lasciare il cervello e inibisce l’ingresso di nutrienti come il glucosio. Forse ancora più dannosa, la barriera disfunzionale consente alle cellule e alle molecole infiammatorie del corpo di entrare e danneggiare il cervello.
“La ricerca, il primo studio longitudinale ad utilizzare una genomica così avanzata, fornisce ora ai ricercatori un nuovo obiettivo per l’intervento terapeutico nella malattia di Parkinson”, afferma l’autore senior dello studio, Charbel Moussa, MBBS, Ph.D., Direttore della Neuroterapia traslazionale del Centro medico.
La nuova scoperta proviene dalla seconda parte di uno studio clinico di Fase II che ha caratterizzato il sequenziamento dell’intero genoma di nuova generazione del liquido cerebrospinale di 75 pazienti con Parkinson, prima e dopo il trattamento con un farmaco per la leucemia riproposto, Nilotinib o un placebo.
Questo studio è durato 27 mesi; lo studio iniziale era in doppio cieco e i pazienti sono stati randomizzati a ricevere placebo o 150 mg o 300 mg di Nilotinib per 12 mesi. I pazienti avevano una grave malattia di Parkinson; tutti trattati con standard di cura ottimali e molti (30%) avevano utilizzato anche i trattamenti più sofisticati possibili, come la stimolazione cerebrale profonda. La seconda parte dello studio ha utilizzato un design adattivo e tutti i partecipanti hanno avuto un periodo di sospensione del farmaco di 3 mesi prima della nuova randomizzazione a 150 mg o 300 mg per altri 12 mesi. Dopo 27 mesi, Nilotinib è risultato sicuro e i pazienti che hanno ricevuto Nilotinib hanno mostrato un aumento dose-dipendente della dopamina, la sostanza chimica persa a causa della distruzione neuronale.
“Sembrava che Nilotinib avesse arrestato il declino motorio e non motorio nei pazienti che assumevano la dose maggiore di 300 mgr“, afferma Moussa.
I risultati clinici di questo studio sono stati pubblicati su Movement Disorders nel marzo 2021.
La parte attuale dello studio, appena pubblicata, ha esaminato il liquido cerebrospinale dei pazienti tramite l’epigenomica, che è un’analisi sistematica dello stato globale dell’espressione genica, in correlazione con i risultati clinici continui. La nuova analisi aiuta a spiegare i risultati clinici.
Vedi anche:Parkinson: smentita l’efficacia degli antiossidanti
Nilotinib ha inattivato una proteina (DDR1) che stava distruggendo la capacità della barriera ematoencefalica di funzionare correttamente. Quando la DDR1 è stata inibita, è ripreso il normale trasporto di molecole dentro e fuori dal filtro cerebrale e l’infiammazione è diminuita al punto che la dopamina, il neurotrasmettitore impoverito dal processo patologico, è stata nuovamente prodotta.
Moussa e il suo team hanno lavorato a lungo sugli effetti che Nilotinib (Tasigna) può avere sulla neurodegenerazione, compreso il morbo di Alzheimer e il morbo di Parkinson. Il farmaco è stato approvato nel 2007 per la leucemia mieloide cronica (LMC), ma Moussa ha sostenuto che il suo meccanismo d’azione può aiutare il cervello a distruggere le tossine che si sviluppano nel cervello dei pazienti con disturbi neurodegenerativi.
“Non solo Nilotinib attiva il sistema di smaltimento dei rifiuti del cervello per eliminare le proteine tossiche cattive, ma sembra anche riparare la barriera ematoencefalica per consentire a questi rifiuti tossici di lasciare il cervello e consentire l’ingresso di sostanze nutritive”, spiega Moussa. “Si ritiene generalmente che la malattia di Parkinson implichi deficit mitocondriali o energetici che possono essere causati da tossine ambientali o dall’accumulo di proteine tossiche; non è mai stata identificata come una malattia vascolare”.
“Per quanto ne sappiamo, questo è il primo studio a dimostrare che la barriera ematoencefalica del corpo offre potenzialmente un obiettivo per il trattamento del morbo di Parkinson“, afferma Moussa. “Rimane molto lavoro da fare, ma il solo fatto di sapere che il sistema vascolare cerebrale di un paziente sta svolgendo un ruolo significativo nella progressione della malattia è una scoperta molto promettente“.
Fonte: Neurology Genetics