(Alzheimer-Immagine Credit Public Domain).
Un team internazionale di scienziati ha scoperto una mutazione genetica legata all’insorgenza precoce del morbo di Alzheimer, tracciando il difetto del DNA attraverso più membri di una singola famiglia.
L’Alzheimer è noto da tempo come una malattia che deruba la mente, che cancella i ricordi e distrugge il senso di sé. La maggior parte dei casi insorgono sporadicamente, emergono dopo i 65 anni, trasmutando i propri anni d’oro in un incubo segnato da una malattia cerebrale incurabile.
A parte la demenza di Alzheimer che inizia sporadicamente nella vecchiaia, ci sono forme familiari insidiose che iniziano anni o decenni prima. L’esordio precoce si riferisce all’Alzheimer che inizia prima dei 65 anni.
Ora, un team internazionale di scienziati, guidato da neurobiologi in Svezia, ha identificato una forma straordinariamente rara della malattia che finora è stata riscontrata solo in una famiglia. Questa forma di Alzheimer è aggressiva, rapida e ruba gli anni più produttivi delle sue vittime attraverso le loro funzioni cognitive.
Spiegano gli autori:
“Il gene della proteina precursore dell’amiloide (APP) codifica per la proteina precursore dell’amiloide, la cui proteolisi dà origine ai peptidi Aβ. Le mutazioni nell’APP causano la malattia di Alzheimer (AD) familiare. In questo studio, descriviamo una delezione di APP patogena che causa una forma dominante di AD. Questa mutazione, chiamata mutazione APP di Uppsala, determina un esordio precoce e una rapida progressione dell’AD. A livello molecolare, la mutazione APP Uppsala altera l’elaborazione delle proteine, determinando un aumento della produzione di Aβ e una rapida aggregazione. I risultati contribuiscono a chiarire i meccanismi molecolari che regolano lo sviluppo della AD e a comprendere l’impatto delle mutazioni di APP sulla fisiopatologia della malattia“.
Ricercatori in Svezia hanno chiamato questa forma di Alzheimer, la delezione dell’APP Uppsala, in onore della famiglia che è dotata di questo famigerato errore del DNA che provoca la discesa nella demenza in giovane età.
“Gli individui affetti hanno un’età all’inizio dei sintomi intorno ai quarant’anni e soffrono di un decorso della malattia in rapida progressione”, ha affermato la Dott.ssa María Pagnon de la Vega, scrivendo sulla rivista Science Translational Medicine. Insieme ai suoi colleghi del Dipartimento di sanità pubblica e scienze dell’assistenza all’Università di Uppsala in Svezia, Pagnon de la Vega ha collaborato con un ampio team di neuroscienziati, biologi strutturali e molecolari ed esperti di imaging in tutta Europa. I ricercatori hanno utilizzato più strumenti all’avanguardia per individuare un difetto che ha un ruolo di primo piano nel destino di una famiglia. Hanno scoperto che la mutazione accelera la formazione di placche proteiche dannose per il cervello, note come beta amiloide o più semplicemente come Aβ. Le placche appiccicose distruggono i neuroni e, di conseguenza, annullano le funzioni esecutive del cervello stesso. I neuroscienziati definiscono fondamentalmente le funzioni esecutive come memoria di lavoro, flessibilità mentale e autocontrollo.
Altre forme di Alzheimer sono state collegate a mutazioni nel gene APP, ma questa è una delezione che Pagnon de la Vega e colleghi hanno confermato attraverso analisi genetiche, ricerche biologiche strutturali, studi sulla chimica degli amminoacidi e delle proteine e spettrometria di massa per caratterizzare l’amiloide. —la proteina deleteria—che pervade il tessuto cerebrale dei portatori di mutazioni.
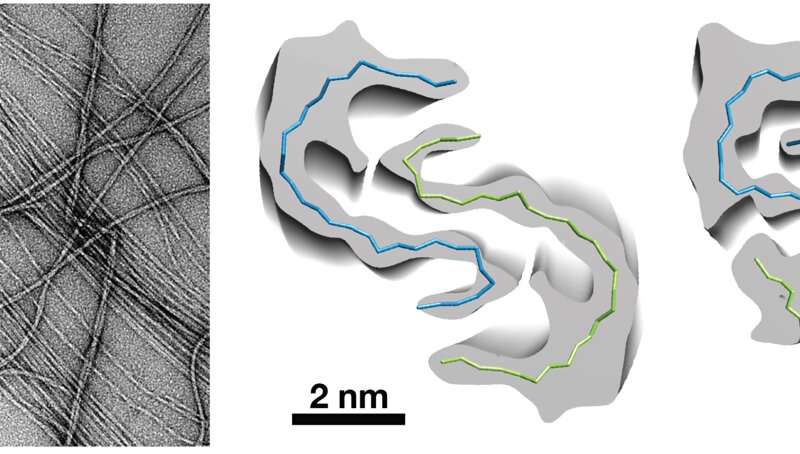
Nel caso dei portatori, tutti avevano una delezione in una specifica stringa di amminoacidi che fanno parte della proteina precursore dell’amiloide. Gli amminoacidi, mancano. Immagina una collana di perle resa significativamente più corta come risultato di sei perline mancanti.
Le “perline” di amminoacidi non sono nel filamento perché il gene APP in questa famiglia svedese non le codifica. In termini numerici, la delezione taglia una striscia di sei amminoacidi, con conseguenti depositi distruttivi di proteina Aβ in tutto il cervello.
La storia della famiglia dietro la scoperta genetica è iniziata sette anni fa in Svezia, quando due fratelli si sono recati in una clinica per i disturbi della memoria presso l’Ospedale universitario di Uppsala, dove sono stati valutati per problemi di memoria. A soli 40 e 43 anni all’epoca, i fratelli, purtroppo, non erano gli unici le cui menti erano confuse e in disfacimento. Un altro parente della loro età stava sperimentando sintomi quasi identici.
Un cugino si è rivolto con i fratelli alla stessa clinica per i disturbi della memoria che stavano soffocando la loro capacità di parlare con frasi chiare e ponderate e cancellando la capacità di eseguire semplici calcoli. A tutti e tre è stata diagnosticata la malattia di Alzheimer ad esordio precoce. Eppure questo trio non era solo nel declino cognitivo familiare.
I medici avevano curato il padre dei due fratelli due decenni prima. Aveva anche 40 anni quando inizialmente sono emersi i sintomi. I medici hanno valutato il padre nella stessa clinica per i disturbi della memoria dove i suoi figli erano diventati malati di Alzheimer.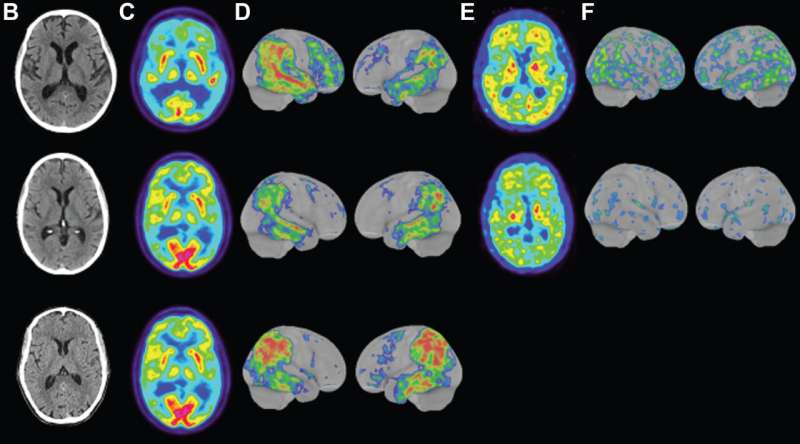
Immagine:TC del cervello di due fratelli e un cugino con malattia di Alzheimer familiare che ospitava la mutazione APP Uppsala. Credito: M. Pagnon de la Vega et al., Science Translational Medicine (2021)
Nel momento in cui i due fratelli e il cugino sono arrivati alla clinica per i disturbi della memoria, erano tutti gravemente sintomatici. Avevano problemi a parlare e avevano perso la capacità di eseguire semplici calcoli. I medici hanno anche stabilito che stavano chiaramente avendo problemi con le funzioni esecutive e le scansioni cerebrali hanno rivelato i segni distintivi dell’Alzheimer in tutti e tre. Le scansioni cerebrali hanno rivelato prove di atrofia nelle regioni frontoparietale e mediotemporale del cervello. I punteggi al Mini Mental State Examination, una valutazione frequentemente somministrata agli anziani per testare le capacità cognitive, non erano solo bassi, ma in un intervallo solitamente osservato negli anziani con disabilità cognitiva. Tutti erano ancora sulla quarantina al momento del test.
Pagnon de la Vega e colleghi definiscono questa forma di Alzheimer come autosomica dominante, trasmessa da una generazione all’altra e che si muove rapidamente in discesa. Non ci sono dati che suggeriscano che altre famiglie siano portatrici della delezione dell’APP di Uppsala, sebbene in Svezia siano state identificate altre forme di Alzheimer familiare.
Vedi anche:Alzheimer: l’infiammazione la chiave per la progressione
“I sintomi e i biomarcatori sono tipici della malattia di Alzheimer, ad eccezione del normale liquido cerebrospinale”, ha scritto Pagnon de la Vega, il primo autore dello studio, riferendosi alla delezione dell’APP di Uppsala.
Prima della scoperta della delezione, più di 50 altre mutazioni del gene APP erano state identificate in tutto il mondo e sono associate all’insorgenza precoce dell’Alzheimer. Le mutazioni APP, in generale, sono responsabili di meno del 10% di tutti i casi ad esordio precoce. La delezione dell’APP di Uppsala è la prima delezione di più aminoacidi che porta all’insorgenza precoce dell’Alzheimer.
La malattia di Alzheimer, sporadica o genetica, non ha cura ed è responsabile di 355 miliardi di dollari di costi totali ogni anno solo negli Stati Uniti, secondo i dati dell’Alzheimer’s Association.
A meno che non si trovi una cura, si prevede che il disturbo travolgerà i sistemi sanitari globali entro il 2050 a causa dell’inesorabile invecchiamento della popolazione, secondo l’Organizzazione Mondiale della Sanità.
Fonte: Science

