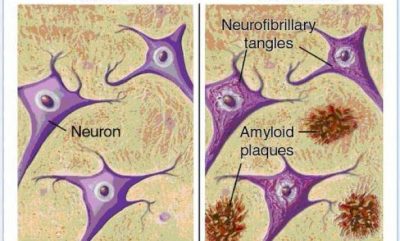
In un importante passo avanti, i ricercatori del Massachusetts General Hospital (MGH) hanno scoperto come la beta amiloide, la neurotossina che si ritiene essere alla radice del morbo di Alzheimer (AD), si formi negli assoni e nelle strutture correlate che collegano i neuroni nel cervello, dove provoca il maggior danno.
I loro risultati, pubblicati su Cell Reports, potrebbero servire da guida per lo sviluppo di nuove terapie per prevenire l’insorgenza di questa devastante malattia neurologica.
Tra i suoi numerosi contributi alla ricerca sull’AD, Rudolph Tanzi, Ph.D., vice-Presidente di Neurologia e co-Direttore del McCance Center for Brain Health presso MGH, ha guidato un team nel 1986 che ha scoperto il primo gene della malattia di Alzheimer, noto come APP che fornisce istruzioni per la produzione di proteine amiloideprecursori (APP). Quando questa proteina viene tagliata (o scissa) dagli enzimi, prima la beta secretasi, seguita dalla gamma secretasi, il sottoprodotto è la beta amiloide. Si ritiene che grandi depositi di beta amiloide causino la distruzione neurologica che si traduce in AD. La beta amiloide che si forma negli assoni e nelle terminazioni nervose del cervello causa il peggior danno nell’AD compromettendo la comunicazione tra le cellule nervose (o neuroni) nel cervello. I ricercatori di tutto il mondo hanno lavorato intensamente per trovare modi per bloccare la formazione di beta amiloide prevenendo la scissione da parte della beta secretasi e della gamma secretasi. Tuttavia, questi approcci sono stati ostacolati da problemi di sicurezza.
Vedi anche:Alzheimer: perchè alcuni neuroni muoiono e altri no?
Nonostante anni di ricerca, la beta amiloide è rimasta un grande mistero. “Sapevamo che è prodotta negli assoni delle cellule nervose del cervello, ma non sapevamo come”, dice Tanzi. Lui ed i suoi colleghi hanno sondato la questione studiando il cervello dei topi utilizzando un modello di coltura cellulare tridimensionale della malattia creato nel 2014 da Tanzi e dal collega, Doo Yeon Kim, Ph.D. In precedenza, nel 2013, molti altri ricercatori MGH, tra cui la neurobiologa Dora Kovacs, Ph.D. (che è sposata con Tanzi) e Raja Bhattacharyya, Ph.D., un membro del laboratorio di Tanzi, hanno dimostrato che una forma di APP che ha subito un processo chiamato palmitoilazione (palAPP) dà origine alla beta amiloide. Quello studio ha indicato che, all’interno del neurone, palAPP viene trasportato in una vescicola (o sacca) grassa nota come zattera lipidica. Ma ci sono molte forme di lipid raft. “Quindi la domanda era: quali zattere lipidiche sono coinvolte? E quali sono le più rilevanti per i processi neuronali che costituiscono le reti neurali del cervello?“, dice Tanzi.
La nuova indagine ha rivelato che palAPP è stabilizzato e preparato per la scissione dalla beta secretasi in speciali zattere lipidiche all’interno del neurone nelle membrane del reticolo endoplasmatico associato ai mitocondri (MAM). “Abbiamo dimostrato per la prima volta non solo che MAM è il luogo in cui palAPP viene elaborato dalla beta secretasi per produrre beta-amiloide, ma che ciò accade esclusivamente negli assoni e nei processi neuronali in cui Abeta fa la maggior parte dei suoi danni“, afferma Bhattacharyya, autore principale dell’articolo pubblicato da Cell Reports. Questo ruolo del reticolo endoplasmatico associato ai mitocondri era precedentemente sconosciuto, sebbene ricerche precedenti indicassero che palAPP sono aumentati in numero e attività nel cervello delle persone con malattia di Alzheimer.
Successivamente, il team MGH ha voluto sapere cosa succede quando i livelli e l’attività MAM sono stati intenzionalmente alterati. I ricercatori hanno dimostrato per la prima volta che la prevenzione dell’assemblaggio di MAM, con la terapia genica o con un farmaco che bloccava una proteina chiave chiamata recettore sigma-1 (S1R), riduceva drasticamente la scissione della beta secretasi di palAPP negli assoni e riduceva la produzione di beta-amiloide. Al contrario, un farmaco che ha attivato S1R ha innescato un aumento della scissione della beta secretasi di palAPP e una maggiore produzione di beta amiloide negli assoni.
Vedi anche:Alzheimer: drenaggio dei detriti cerebrali migliora le terapie
“I nostri risultati suggeriscono che il recettore sigma-1 potrebbe essere un obiettivo terapeutico praticabile per ridurre la produzione di Abeta, in particolare negli assoni“, afferma Tanzi. Lo studio supporta anche una strategia già in esame da Tanzi e dal suo team, che sta sviluppando un trattamento sperimentale che inibisce la palmitoilazione di APP, il processo che produce palAPP. È anche noto che un’altra classe di farmaci che Kovacs sta studiando per prevenire la formazione di beta amiloide, chiamati inibitori ACAT, funziona direttamente in MAM. In futuro, questi e altri interventi che ostacoleranno la produzione di questo pool più pericoloso di beta amiloide assonale potrebbe essere utilizzato insieme alla diagnosi precoce (attraverso esami del sangue o di imaging) per arrestare o rallentare la progressione dell’AD.