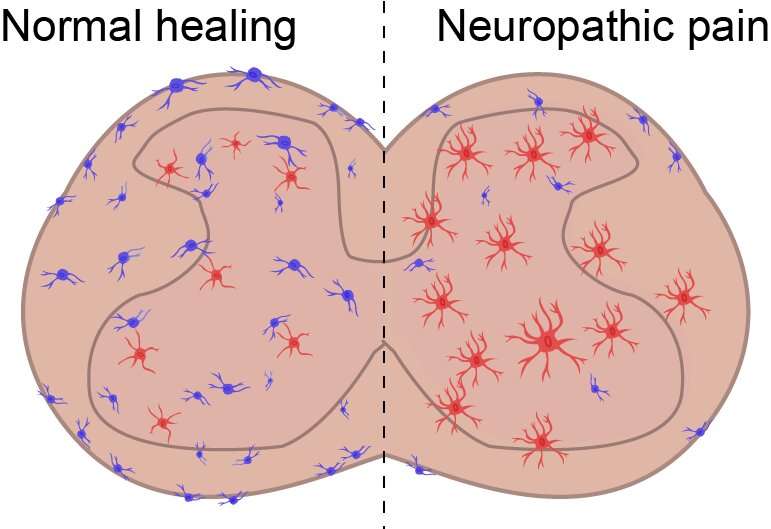
(Dolore cronico-immagine: illustrazione del midollo spinale di cellule pro-infiammatorie (rosse) e macrofagi MRC1 + antinfiammatori (blu). Credito: Zylka Lab, UNC School of Medicine).
Uno dei tratti distintivi del dolore cronico è l’infiammazione e gli scienziati della UNC School of Medicine hanno scoperto che le cellule antinfiammatorie chiamate macrofagi MRC1 + sono disfunzionali in un modello animale di dolore neuropatico. Riportare queste cellule al loro stato normale potrebbe offrire un percorso per il trattamento del dolore debilitante causato da danni ai nervi o da un malfunzionamento del sistema nervoso.
I ricercatori, che hanno pubblicato il loro lavoro su Neuron, hanno scoperto che stimolando l’espressione di una proteina antinfiammatoria chiamata CD163 si riducono i segni di neuroinfiammazione nel midollo spinale dei topi con dolore neuropatico.
“I macrofagi sono un tipo di cellula immunitaria che si trova nel sangue e nei tessuti di tutto il corpo. Abbiamo trovato una classe di macrofagi antinfiammatori che normalmente aiutano il corpo a risolvere il dolore. Ma il dolore neuropatico sembra disabilitare questi macrofagi e impedire loro di fare il proprio lavoro”, ha detto l’autore senior dello studio Mark Zylka, Ph.D., Direttore dell’UNC Neuroscience Center e Kenan Distinguished Professor of Cell Biology and Physiology. “Fortunatamente questi macrofagi non sembrano essere permanentemente disabili, poiché siamo stati in grado di convincerli a intensificare le loro azioni antinfiammatorie e ridurre il dolore neuropatico. Siamo convinti che sarà possibile sviluppare nuovi trattamenti per il dolore potenziando le attività di questi macrofagi”.
Secondo i Centers for Disease Control and Prevention, circa un quinto della popolazione statunitense soffre di dolore cronico. Spesso le cause sottostanti sono sfuggenti e i pazienti hanno bisogno di alleviare il dolore per poter condurre una vita normale. Sebbene gli oppioidi siano ottimi nel trattamento del dolore a breve termine, questi farmaci possono avere gravi effetti collaterali se usati per periodi prolungati, come dipendenza, depressione respiratoria, vertigini, nausea e morte per sovradosaggio.
Uno dei motivi per cui gli analgesici forti funzionano bene, ma possono avere effetti collaterali drammatici, ha a che fare con un fatto biologico di base: il dolore coinvolge un insieme molto diversificato di cellule e i trattamenti attuali mancano di specificità del tipo di cellula. Quindi, qualsiasi dato farmaco può risolvere cambiamenti avversi in alcune cellule per alleviare il dolore, ma il farmaco potrebbe esacerbare una particolare funzione in altre cellule, portando a effetti collaterali negativi.
Con una tecnologia emergente chiamata sequenziamento dell’RNA a cellula singola, gli scienziati possono ora interrogare migliaia di cellule contemporaneamente per vedere quali cellule vengono alterate durante il dolore cronico e in che modo le cellule cambiano.
Vedi anche:Dolore cronico: nuovo trattamento senza oppioidi
“Sapere quali cellule prendere di mira ci permette di progettare terapie molto specifiche. Le terapie mirate in teoria dovrebbero avere meno effetti collaterali negativi“, ha detto Jesse Niehaus, studente laureato nel laboratorio Zylka e primo autore del documento pubblicato in Neuron.
Per capire quali cellule stavano cambiando e in che modo, il laboratorio di Zylka ha eseguito il sequenziamento dell’RNA a cellula singola sul midollo spinale di topi con dolore neuropatico, un tipo di dolore cronico causato da danni ai nervi. Il midollo spinale subisce molti cambiamenti a lungo termine che contribuiscono al dolore neuropatico. Da quegli esperimenti, i ricercatori hanno trovato una popolazione di cellule antinfiammatorie chiamate macrofagi MRC1 + che erano disfunzionali.
“Questa scoperta è stata incredibilmente interessante perché l’infiammazione a lungo termine nel midollo spinale è comunemente vista negli animali con dolore neuropatico”, ha detto Niehaus.
Una volta rivelata l’identità delle cellule, il laboratorio di Zylka ha fornito una terapia genica progettata per stimolare l’espressione di una proteina antinfiammatoria chiamata CD163 nei macrofagi MRC1 +. Con questo approccio, un singolo trattamento ha ridotto l’infiammazione del midollo spinale e alleviato il comportamento correlato al dolore fino a un mese.
“Questa scoperta è piuttosto eccitante”, ha detto Zylka, “poiché suggerisce immediatamente più modi distinti per potenziare la funzione di questi macrofagi. Ognuno di questi approcci terapeutici potrebbe fornire un modo più preciso per trattare il dolore neuropatico”.