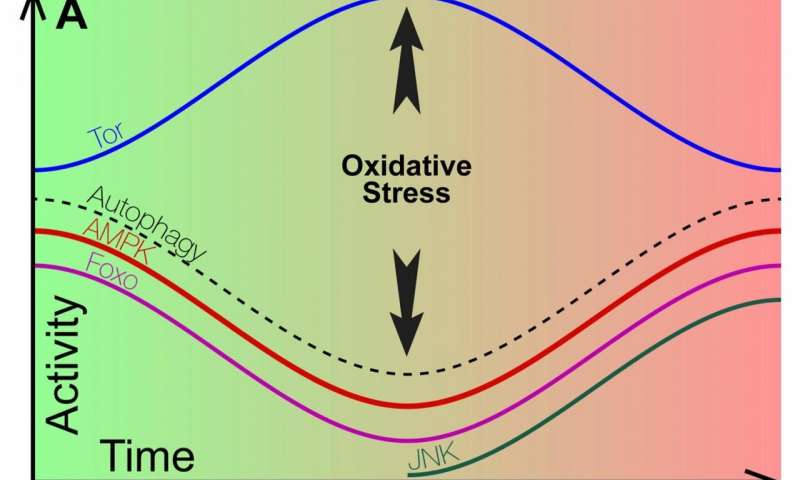
Immagine:neurodegenerazione. Sulla base di migliaia di esperimenti nell’arco di più di un decennio, i biochimici della Rice University Michael Stern e James McNew ritengono che malattie degenerative così varie come l’Alzheimer, il Parkinson e l’atrofia muscolare si manifestino in due fasi (verde e rossa) contrassegnate da distinte alterazioni nell’attività della segnalazione, proteine del percorso TOR, AMPK, Foxo e JNK. Nella fase iniziale (a sinistra), l’autofagia viene soppressa, il che aumenta lo stress ossidativo, determinando infine la fase tardiva (a destra) in cui l’autofagia viene ripristinata, causando una rapida degenerazione. Credito: Michael Stern / Rice University
I biochimici della Rice University Michael Stern e James McNew hanno studiato come la neurodegenerazione uccide le cellule. Hanno condotto innumerevoli esperimenti in più di un decennio e hanno riassunto tutto ciò che hanno imparato in un semplice diagramma che sperano possa cambiare il modo in cui i medici percepiscono e trattano le malattie degenerative diverse come l’Alzheimer, il Parkinson e l’atrofia muscolare.
In uno studio pubblicato questo mese su Molecular Psychiatry, McNew e Stern propongono che la degenerazione, a livello cellulare, avviene in due fasi distinte che sono contrassegnate da attività molto diverse delle vie di segnalazione delle proteine che regolano le funzioni cellulari di base.
“Vorremmo che i medici e altri ricercatori capissero che le due fasi della degenerazione rappresentano entità distinte, con alterazioni distinte nei percorsi di segnalazione che hanno effetti distinti sulla patologia della malattia“, ha detto Stern. “In altre parole, pensiamo che i pazienti debbano essere trattati in modo diverso a seconda della fase in cui si trovano”.
Il diagramma di Stern e McNew mostra come l’attività delle proteine di segnalazione delle cellule chiave aumenti o diminuisca all’inizio della degenerazione, determinando in ultima analisi lo stress ossidativo. A sua volta, lo stress ossidativo determina quindi la seconda fase della condizione, durante la quale avviene la degenerazione, dove le proteine di segnalazione implicate nella prima fase si comportano in modo completamente diverso.
Poiché le cellule si comportano in modo abbastanza diverso nelle due fasi, la ricerca suggerisce che i pazienti nelle diverse fasi di una malattia possono rispondere in modo diverso allo stesso trattamento.
Vedi anche:Neurodegenerazione e spazzatura nel cervello
“Le due fasi della degenerazione non sono state precedentemente riconosciute, quindi non è stato compreso, clinicamente, che si hanno due diverse popolazioni di pazienti”, ha detto McNew. “Oggi sono trattati come un’unica popolazione e pensiamo che questo abbia confuso gli studi clinici e spieghi perché alcuni studi sull’Alzheimer hanno dato effetti variabili e irriproducibili. Sarebbe come cercare di trattare tutti i pazienti affetti da meningite con antibiotici senza rendersi conto che ci sono due tipi di meningite, una batterica e una virale “.
Stern e McNew, professori di biochimica e biologia cellulare presso il Dipartimento di BioScienze della Rice, si sono interessati ai processi cellulari dei disturbi neurodegenerativi quando hanno iniziato a studiare la paraplegia spastica ereditaria (HSP) alla fine degli anni 2000. Una malattia rara, la HSP è caratterizzata da intorpidimento e debolezza delle gambe e dei piedi a causa del progressivo deterioramento dei neuroni che collegano la colonna vertebrale e la parte inferiore della gamba.
McNew e Stern hanno utilizzato esperimenti sui moscerini della frutta per mettere insieme sistematicamente l’effetto domino biochimico che ha causato la progressiva perdita di neuroni. Si pensava che il danno ai nervi potesse portare all’atrofia muscolare, ma i loro studi hanno scoperto che le cellule muscolari attaccate ai neuroni hanno iniziato a degenerare dallo stesso tipo di cascata biochimica prima che le cellule nervose morissero.
Un attore chiave nella cascata è stata una proteina chiamata TOR, un regolatore principale della crescita cellulare e una proteina essenziale per tutta la vita di ordine superiore, dal lievito all’uomo. TOR agisce come una manopola, aumentando o diminuendo la crescita in base alle condizioni che una cellula sta vivendo. In alcune condizioni, una crescita elevata è garantita e vantaggiosa e in altre situazioni la crescita deve essere ridotta in modo che l’energia e le risorse possano essere conservate per le attività quotidiane, come il riciclaggio o la riparazione che avvengono durante un processo noto come autofagia.
Alcuni tipi di cancro assumono TOR per promuovere la crescita cellulare aggressiva e l’aumento dell’attività TOR è stato anche implicato in disturbi neurodegenerativi come il morbo di Alzheimer e Parkinson e in malattie contrassegnate da atrofia muscolare. Dopo aver raccolto prove su come TOR e molte altre proteine di segnalazione si sono comportate nella neurodegenerazione, McNew e Stern hanno vinto una sovvenzione dal National Institute of Neurological Disorders and Stroke nel 2018 per esperimenti volti a indagare i cambiamenti del percorso di segnalazione che si verificano nelle prime fasi della degenerazione.
“All’epoca, pensavamo che potesse esserci una fase tardiva nella neurodegenerazione durante la quale si verifica effettivamente la degenerazione, ma non abbiamo proposto alcun esperimento per verificarlo”, ha detto Stern. “Nel nuovo articolo, siamo espliciti sull’esistenza di una fase tardiva perché la degenerazione si verifica solo durante questa fase e abbiamo trovato anche abbondanti ricerche a sostegno“.
Stern ha spiegato che il processo in due fasi descritto nello studio “è il motore di base” che spinge in avanti la maggior parte o anche tutte le forme di degenerazione. Tuttavia, in aggiunta, ci sono anche input il cui ruolo è specificare la velocità con cui il motore gira.
“Per comprendere la neurodegenerazione, è fondamentale capire come funzionano questi input”, ha detto il ricercatore. Ad esempio, l’insulino-resistenza gioca un ruolo ben noto nella guida della malattia di Alzheimer e nello studio McNew e Stern descrivono come lo fa accelerando la progressione attraverso la fase iniziale.
“Allo stesso modo, i nostri dati suggeriscono che la diminuzione della trasmissione sinaptica, come avviene nel nostro modello di insetto HSP, innesca allo stesso modo la degenerazione accelerando la progressione attraverso la fase iniziale“, ha detto McNew. “La nostra borsa di studio NIH è stata finanziata in modo che potessimo apprendere il meccanismo con cui ciò si verifica”.
Ora che hanno dimostrato chiaramente che esistono due fasi di degenerazione, Stern e McNew vorrebbero condurre più esperimenti per vedere come gli effetti di geni specifici sulla degenerazione vengono alterati quando vengono attivati nelle fasi iniziali e finali.
“Quello che vorremmo fare negli ultimi due anni della sovvenzione è ottenere dati per testare alcune delle previsioni che abbiamo fatto, il che aiuterà a determinare se le idee che abbiamo presentato sono corrette”, ha detto Stern.
Fonte:Molecular Psychiatry