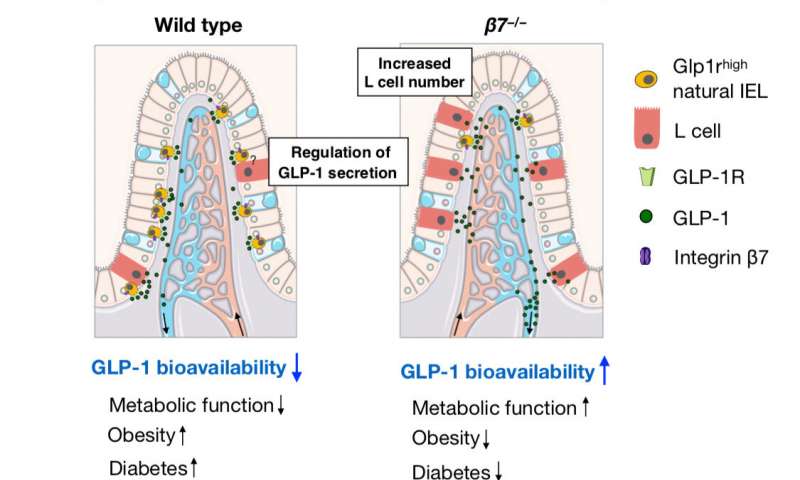
Immagine: Le cellule immunitarie intestinali svolgono un ruolo chiave nella regolazione metabolica e nella salute cardiovascolare. Immagini affiancate del piccolo intestino confrontano la presenza di cellule che regolano il metabolismo. Credito: Servier Medical Art.
Un gruppo di ricerca del Massachusetts General Hospital (MGH) ha identificato quello che sembra essere un importante checkpoint nel metabolismo alimentare, un gruppo di cellule nell’intestino tenue che rallenta il metabolismo, aumentando la quantità di cibo ingerito che viene immagazzinato come grasso anziché essere rapidamente convertito in energia.
Nel rapporto pubblicato su Nature, i ricercatori scoprono che i topi privi di queste cellule possono consumare diete ricche di grassi e zuccheri senza sviluppare condizioni come obesità, diabete, ipertensione e malattie cardiache.
Dopo aver mangiato, il tuo corpo può convertire l’energia in calore e bruciarla rapidamente o può convertire il cibo in grasso e conservarlo per un uso successivo”, dice Filip Swirski, del MGH Center for Systems Biology, autore senior dell’articolo. “Parliamo spesso di persone che hanno un ‘alto metabolismo‘ e sembrano essere in grado di mangiare quello che vogliono senza ingrassare, mentre altre lottano con l’obesità. Queste cellule, che sono note per la loro funzione nel sistema immunitario, sembrano anche svolgere un ruolo importante in quella scelta metabolica“.
Lo studio del team si è concentrato su una proteina chiamata integrina β7 che non è nota per avere influenza sul metabolismo. Il team di MGH inizialmente ha scoperto che i topi privi del gene per l’integrina β7, alimentati con una dieta normale, hanno acquisito quantità uguali di peso rispetto a un gruppo di animali di controllo, anche se gli animali β7 negativi mangiavano più cibo ed erano altrettanto attivi. I test metabolici hanno indicato che i topi β7 negativi hanno convertito più cibo in energia, suggerendo che avevano un metabolismo basale più alto. Inoltre hanno bruciato più glucosio nel grasso bruno, erano più tolleranti al glucosio, avevano livelli di trigliceridi più bassi e una tolleranza al grasso migliore rispetto ai topi di controllo.
Per verificare se questi benefici persistessero in condizioni nutrizionali note per indurre la sindrome metabolica – un gruppo di sintomi associati al diabete di tipo 2 e alle malattie cardiovascolari – i ricercatori hanno alimentato sia topi β7-negativi che topi di controllo con una dieta ricca di grassi, zuccheri e sodio.
I topi β7 negativi sono rimasti magri, tolleranti al glucosio e non hanno sviluppato ipertensione o altri risultati tipici di una dieta ricca di grassi. I topi di controllo sono diventati obesi, con pressione sanguigna elevata e ridotta tolleranza al glucosio.
In esperimenti con un modello di topo geneticamente programmato per sviluppare colesterolo elevato, i ricercatori hanno scoperto che il blocco dell’espressione di β7 nel midollo osseo, dove sono generate le cellule immunitarie, manteneva normali livelli lipidici negli animali, nonostante fossero alimentati con una dieta ricca di colesterolo. I topi con β7 negativo espellevano più colesterolo, avevano migliorato la tolleranza al glucosio e avevano meno probabilità di sviluppare placche arteriose e altri fattori di rischio cardiovascolare rispetto agli animali con normale espressione di β7 nel midollo osseo.
Una ricerca per le cellule responsabili dell’impatto metabolico di β7 ha rivelato che l’espressione della proteina era più alta in un gruppo di cellule T presenti nel rivestimento dell’intestino tenue. Mentre β7 guida diversi tipi di cellule immunitarie nell’intestino, solo queste cellule T intraepiteliali che esprimono β7 sembrano regolano il metabolismo sistemico. Il team di Swirski ha lo ha dimostrato riducendo i livelli di una proteina chiamata GLP-1, che normalmente aumenta il metabolismo stimolando la secrezione di insulina e l’assorbimento di glucosio.
Swirski ha spiegato che il ruolo di soppressione del metabolismo delle cellule T intraepiteliali β7-positive potrebbe essersi sviluppato per prevenire la fame in condizioni di scarsità di nutrienti. “Nei momenti in cui la disponibilità di cibo è incerta, sarebbe vantaggioso disporre di un sistema che converta parte dell’energia ingerita con il cibo in grasso, ma nei periodi di sovra-alimentazione, un tale sistema può ritorcersi contro e portare alla malattia cardiovascolare che è così diffusa oggi “.
“Restano molte domande a cui dare risposte ed esattamente come queste cellule limitano la disponibilità di GLP-1, se le persone con un metabolismo più elevato hanno meno di queste cellule, come la funzione delle cellule può cambiare nel corso di un giorno o della vita e se il blocco di queste cellule può essere utile nel trattamento di obesità, diabete, ipertensione e aterosclerosi“. Swirski è Professore associato di Radiologia presso la Harvard Medical School.
Fonte, Nature