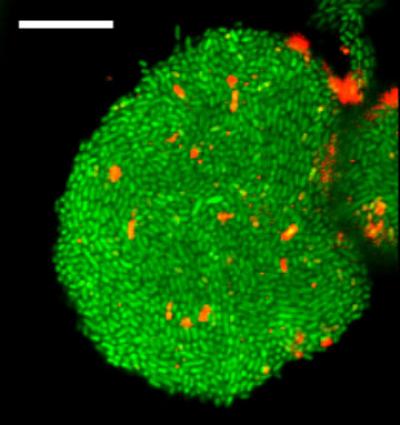
Immagine: questa è un’immagine di cellule che formano un biofilm, una comunità di cellule batteriche protetta dallo stress ambientale e una fonte di resistenza agli antibiotici, in un nuovo dispositivo gel sviluppato nel laboratorio Levchenko.
Riducendo fortemente gli effetti degli antibiotici, la formazione di comunità organizzate di cellule batteriche note come biofilm può essere mortale durante gli interventi chirurgici e nelle infezioni del tratto urinario. I ricercatori della Yale University sono molto vicini alla comprensione di come si sviluppano questi biofilm e di come potenzialmente fermarli.
I biofilm si formano quando le cellule batteriche si raccolgono e sviluppano strutture che le uniscono in una sostanza appiccicosa. Questa colla può proteggere le cellule dal mondo esterno e consentire loro di formare quasi-organismi complessi. I biofilm si possono trovare quasi ovunque, comprese le docce non lavate o le superfici dei laghi. Poiché il guscio protettivo può contrastare i potenziali trattamenti, i biofilm sono più pericolosi quando invadono le cellule umane o si formano su suture e cateteri utilizzati negli ambulatori. Solo negli ospedali americani, migliaia di morti sono attribuiti alle infezioni del sito chirurgico correlate al biofilm e alle infezioni del tratto urinario.
“I biofilm sono un enorme problema medico”, ha detto Andre Levchenko, autore senior dello studio che è stato pubblicato il 5 ottobre in Nature Communications.
La lotta al biofilm è particolarmente difficile perché non è stato ben compreso come le cellule batteriche possano passare dal comportamento individuale alle strutture collettive. Tuttavia, i ricercatori del laboratorio Levchenko, in collaborazione con i colleghi dell’Università della California-San Diego, hanno recentemente trovato un meccanismo chiave per la formazione dei biofilm che fornisce anche un modo per studiare questo processo in modo controllato e riproducibile.
( Vedi anche:Studio rivela come i batteri comunicano in gruppi per evitare gli antibiotici).
I ricercatori hanno progettato e costruito dispositivi microfluidici e nuovi gel che ospitavano cellule uropatogene di E. coli che sono spesso causa di infezioni del tratto urinario. Questi dispositivi hanno mimato l’ambiente all’interno delle cellule umane che ospitano i batteri patogeni durante le infezioni. Gli scienziati hanno scoperto che le colonie batteriche sarebbero cresciute fino al punto in cui sarebbero state schiacciate dalle pareti delle cellule, dalle fibre o dal gel. Questo stress auto-generato era di per sé un fattore scatenante della formazione del biofilm.
“Questo è stato molto sorprendente, ma abbiamo visto tutte le cose che ci si poteva aspettare da un biofilm”, ha detto Levchenko, Professore di ingegneria biomedica John C. Malone e Direttore del Yale Systems Biology Institute. “Le cellule hanno prodotto i componenti del biofilm e sono diventate improvvisamente molto resistenti agli antibiotici e tutto ciò è stato accompagnato dall’indicazione che le cellule erano sottoposte a stress biologico e lo stress derivava da questa interazione meccanica con l’ambiente”.
“Con questa scoperta”, ha detto Levchenko,” i ricercatori possono utilizzare vari dispositivi che imitano altri ambienti cellulari ed esplorare la formazione di biofilm in innumerevoli circostanze. Possono anche utilizzare i dispositivi introdotti in questo studio per produrre biofilm in modo rapido, preciso e in numero elevato, in modo semplice, economico e riproducibile. Ciò consentirebbe la selezione di farmaci che potrebbero potenzialmente violare lo strato protettivo dei biofilm e abbatterli.
“Avere un modello di malattia come questo è d’obbligo quando si vuole fare questo tipo di esperimenti di screening dei farmaci”, ha detto il ricercatore. “Ora possiamo coltivare biofilm in forme e luoghi specifici in modo completamente prevedibile”.
Fonte: EurekAlert