Immagine: Credit: Università di Tokyo.
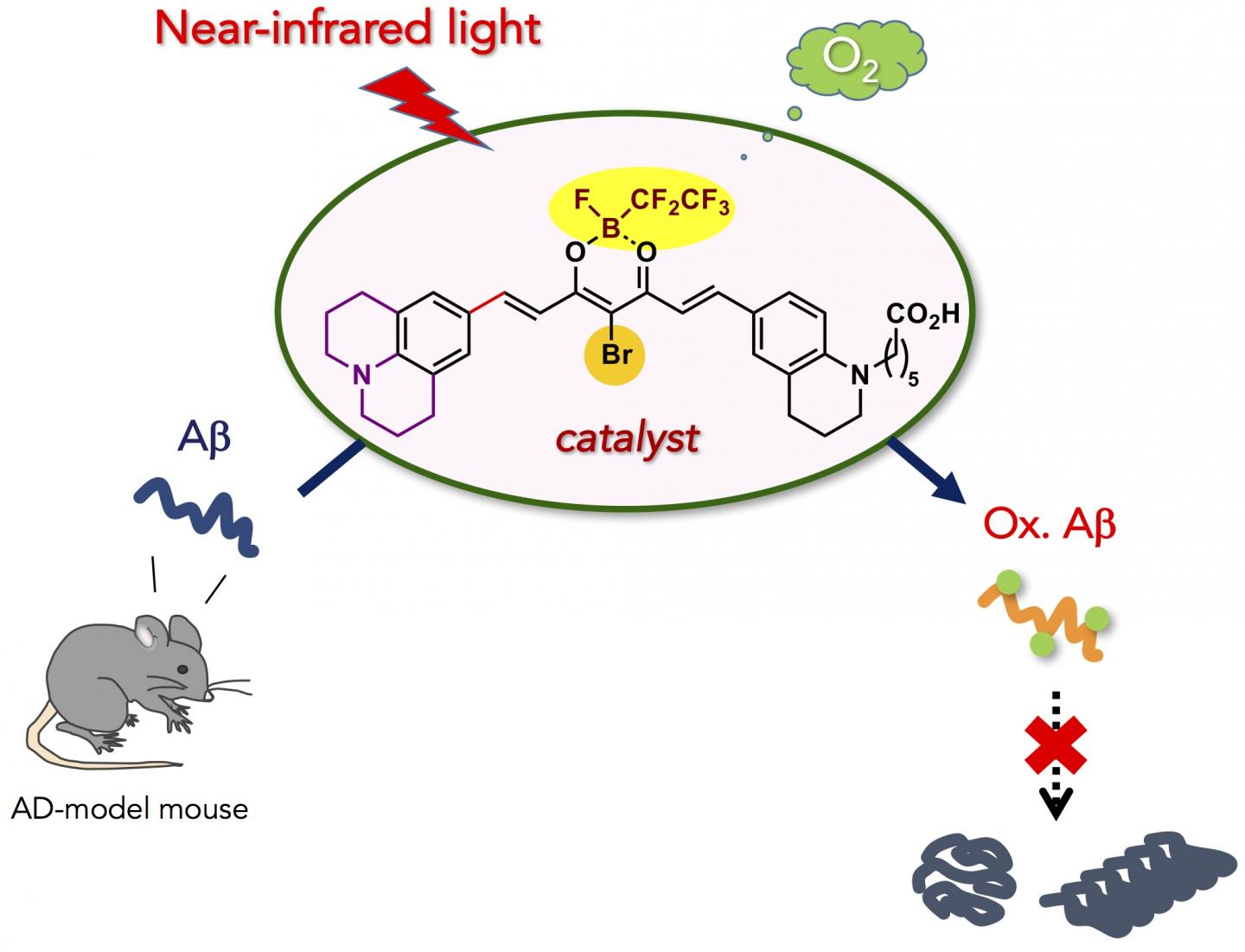
E’ stato sviluppato un nuovo catalizzatore di fotoossigenazione biocompatibile da ricercatori dell’Università di Tokio, che può ossigenare e degradare selettivamente l’aggregazione patogena del peptide amiloide-beta (Aβ) correlato alla malattia di Alzheimer (Aβ) sotto irradiazione luminosa nel vicino infrarosso (NIR). Il catalizzatore è in grado di ossigenare Aβ incorporato sotto la pelle di un topo vivente e di diminuire il livello Aβ nel cervello di topo modello AD. Il nuovo catalizzatore è potenzialmente applicabile al trattamento delle malattie amiloidi periferiche e AD.
L’aggregazione tossica del peptide amiloide e delle proteine è intimamente correlata a un numero di malattie umane. L’amiloide-β (Aβ) è un peptide amiloide rappresentativo la cui aggregazione è correlata alla patogenesi della malattia di Alzheimer (AD). Lo sviluppo di un sistema chimico artificiale che converta selettivamente gli aggregati di amiloide tossici in specie non tossiche in condizioni fisiologiche, potenzialmente sopprimendo il processo patogenetico, potrebbe essere una nuova strategia terapeutica per trattare le malattie amiloidi attualmente incurabili, tra cui l’alzheimer.
Dicono gli autori:
“Abbiamo ipotizzato che l’ossigenazione aerobica fotocatalizzata poteva essere una reazione chimica adatta ad attenuare le proprietà aggregative patogene delle proteine Aβ in condizioni fisiologiche. Poiché l’aggregazione peptidica e proteica dipende generalmente dalle interazioni idrofobiche intermolecolari, l’installazione covalente di atomi di ossigeno idrofili a un peptide o proteina (cioè l’ossigenazione) potrebbe ridurne l’aggregativa. Precedentemente abbiamo riferito che l’ossigenazione aerobica di Aβ procede in presenza di fotocatalizzatori basati su Flavin (vitamina B2) e le proteine Aβ ossigenate risultanti, mostrano una capacità aggregante e una tossicità molto basse. Successivamente, catalizzatori di fotoossigenazione più selettivi, attivati solo nel rilevare una struttura amiloide tossica di ordine superiore, sono stati sviluppati sulla base di una sonda a fluorescenza per il peptide amiloide aggregato e le proteine. Tuttavia, l’applicazione in vivo dei catalizzatori non è stata possibile, poiché l’irradiazione con luce visibile, che ha una bassa penetrazione del tessuto, era necessaria per l’eccitazione del catalizzatore. Per l’applicazione in vivo, i fotocatalizzatori devono essere in grado di funzionare sotto eccitazione con una luce a lunghezza d’onda maggiore, indicata come “finestra ottica” in cui il tessuto vivente assorbe relativamente poca luce.
Qui, abbiamo sviluppato un catalizzatore di fotoossigenazione biocompatibile che può ossigenare selettivamente e degradare l’aggregazione patogena di Aβ sotto irradiazione luminosa nel vicino infrarosso (NIR). Il nuovo catalizzatore mostra quattro vantaggi principali rispetto ai precedenti catalizzatori per la degradazione di Aβ aggregato e tossico: (1) Alta selettività per Aβ aggregato che deriva dall’interruttore on / off di rilevamento della struttura amiloide di ordine superiore per l’attività del catalizzatore. La selettività target precisa consente la fotoossigenazione di Aβ aggregato in presenza delle cellule e nel lisato del cervello di topo. (2) Bassa tossicità per le cellule. L’ottimizzazione strutturale del catalizzatore ha ridotto marcatamente la citotossicità, sia al buio che sotto irradiazione NIR. (3) Elevata potenza di ossigenazione sotto fotoirradiazione NIR. A causa della permeabilità tissutale della luce NIR, la fotoossigenazione di Aβ aggregato sotto la pelle del topo era possibile in alta resa. (4) Applicabilità al cervello degli animali vivi . L’iniezione del catalizzatore sul cervello del topo modello AD e l’irradiazione con luce NIR hanno portato a una significativa diminuzione del livello di Aβ”.
I risultati ottenuti in questo studio rappresentano un passo importante verso l’utilizzo della catalisi artificiale come potenziale strategia terapeutica contro le malattie amiloidi.