Gli scienziati della Northwestern Medicine hanno identificato una cascata tossica che porta alla degenerazione neuronale nei pazienti con malattia di Parkinson (PD) e hanno scoperto come interromperla in uno studio che è stato pubblicato il 7 settembre nella rivista Science.
L’intervento con un trattamento a base di antiossidanti all’inizio dello sviluppo della malattia, può rompere il ciclo degenerativo e migliorare la funzione dei neuroni nel Parkinson, secondo quanto dimostrato dallo studio.
( Vedi anche:Nuovo test può diagnosticare il Parkinson fino a 10 anni prima).
Gli scienziati hanno anche scoperto che i modelli di topi di Parkinson non hanno le stesse anomalie che hanno trovato nei neuroni umani di Parkinson, rivelando l’importanza di studiare i neuroni umani per sviluppare nuove terapie.
Il Dr. Dimitri Krainc, Professore alla Aaron Montgomery e Presidente di neurologia presso la Northwestern University Feinberg School of Medicine, è l’autore senior dello studio. Lena Burbulla, un collega postdottorando del laboratorio di Krainc, è il primo autore.
La ricerca è stata avviata circa sei anni fa nel laboratorio di Krainc presso il Massachusetts General Hospital e la Harvard Medical School ed è stata completata negli ultimi quattro anni a Feinberg.
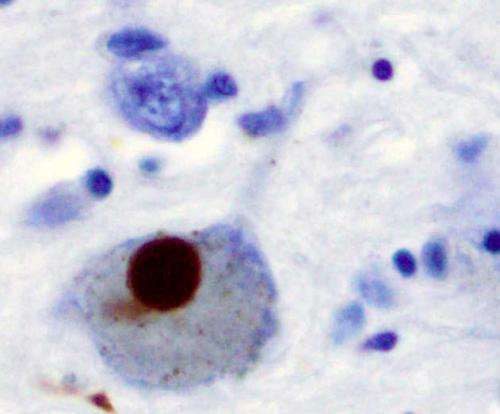
Il Parkinson è il secondo disturbo neurodegenerativo più comune, causato principalmente dalla morte dei neuroni che contengono dopamina nel substantia nigra, regione del cervello coinvolta nel controllo del motore. Mentre le persone perdono naturalmente i neuroni della dopamina mentre invecchiano, i pazienti con Parkinson perdono un numero molto maggiore di questi neuroni e le altre cellule non sono più in grado di compensare la perdita.
“Capire come e perché questi neuroni muoiono è un passo importante per identificare i trattamenti”, ha detto Krainc. “Mentre la ricerca precedente ha indicato che il meccanismo cellulare dietro la morte cellulare coinvolge i mitocondri ed i lisosomi, come questi due percorsi convergono nei neuroni della dopamina per causare la morte cellulare è ancora sconosciuto”, ha aggiunto il ricercatore.
Utilizzando i neuroni umani dai pazienti di Parkinson, Krainc e colleghi hanno identificato una cascata tossica avviata da un accumulo di dopamina ossidata e da una proteina chiamata alfa-sinucleina. In particolare, lo studio attuale ha dimostrato che un accumulo di dopamina ossidata ha depresso l’attività della glucosocerebrosidasi lisosomica (GCase), un enzima implicato nello sviluppo del Parkinson. Quella depressione a sua volta ha indebolito la funzione lisosomica complessiva e ha contribuito alla degenerazione dei neuroni.
L’accumulo della dopamina ossidata non ha però interferito solo con i lisosomi. Krainc ed i suoi colleghi hanno scoperto invece, che la dopamina ossidata ha danneggiato i mitocondri dei neuroni aumentando lo stress ossidativo mitocondriale. Questi mitocondri disfunzionali hanno portato ad aumentare i livelli ossidati della dopamina, creando un ciclo vizioso.
“I percorsi mitocondriali e lisosomiali sono due percorsi critici nello sviluppo delle malattie”, ha dichiarato Krainc, che è anche il Direttore del Centro per le malattie neurologiche rare e Professore di chirurgia neurologica e di fisiologia.
Dopo aver identificato questa cascata tossica, Krainc ed i suoi colleghi hanno cominciato a cercare diversi modi per interromperla.
“Una delle strategie chiave che ha funzionato nei nostri esperimenti è trattare i neuroni della dopamina all’inizio della cascata tossica con antiossidanti specifici che migliorano lo stress ossidativo mitocondriale e la dopamina ossidata“, ha dichiarato Krainc. “Con questo approccio abbiamo scoperto che possiamo attenuare o prevenire gli effetti tossici a valle sui neuroni dopaminergici umani”.
Questo approccio per interrompere la cascata tossica della dopamina ossidata può fornire un obiettivo per lo sviluppo di future terapie. Tuttavia, l’individuazione di pazienti o soggetti con neurodegenerazione in fase precoce può essere difficile, perché i danni si sono spesso verificati molto prima che i sintomi siano evidenti, secondo Krainc.
Di conseguenza, i test genetici saranno centrali per i futuri sforzi diagnostici.
“I geni causali sono i primi candidati per la screening, mentre i geni di rischio come GBA1 sono marcatori meno decisi ma ancora importanti”, ha detto Krainc. “L’individuazione precoce si baserà anche sui test di imaging del cervello e altri significanti clinici”.
È interessante notare che, rispetto ai modelli cellulari umani, i modelli di topi di Parkinson non hanno dimostrato la stessa cascata tossica secondo lo studio. Krainc ed i suoi colleghi hanno dimostrato che ciò è dovuto alle differenze nel metabolismo della dopamina tra le specie e sottolinea l’importanza di studiare i neuroni umani per scoprire nuovi obiettivi per lo sviluppo di farmaci.
Fonte: Science