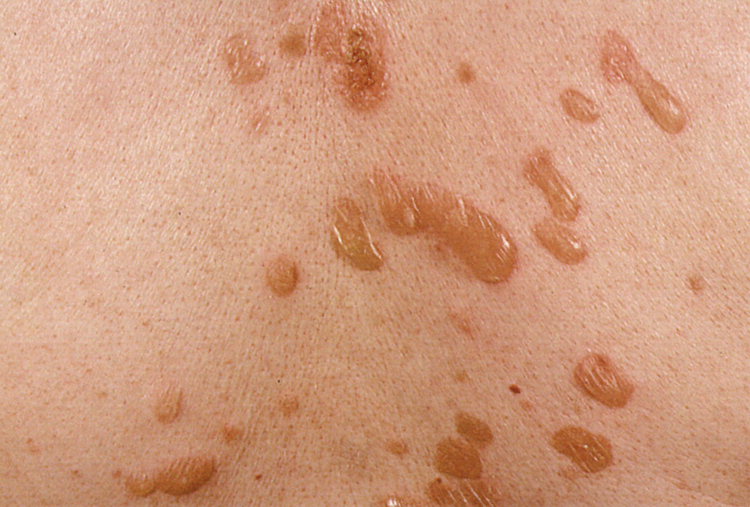
Immagine: pemfigo volgare
In uno studio con potenziali importanti implicazioni per il futuro trattamento di malattie autoimmuni e patologie correlate, gli scienziati della Scuola di Medicina di Perelman all’Università della Pennsylvania hanno trovato un modo per rimuovere il sottogruppo di cellule che producono anticorpi che causano una malattia autoimmune, senza danneggiare il resto del sistema immunitario.
La malattia autoimmune studiata è chiamata pemfigo volgare (PV), una condizione in cui le cellule immunitarie del paziente attaccano una proteina chiamata desmoglein-3 (Dsg3) che si trova normalmente nelle cellule della pelle.
“ Il pemfigo volgare è una malattia della pelle molto grave che provoca la comparsa delle vesciche. E’ una condizione rara. Il pemfigo volgare è più grave rispetto alla maggior parte delle altre malattie della pelle. La maggior parte delle persone con il pemfigo vulgaris muoiono prima che il trattamento venga avviato. Il trattamento avviene di solito con l’uso dei farmaci steroidei e con altri farmaci che sopprimono il sistema immunitario“.
Le attuali terapie per le malattie autoimmuni, come il prednisone e rituximab, sopprimono gran parte del sistema immunitario, lasciando i pazienti vulnerabili alle infezioni potenzialmente fatali e tumori.
( vedi anche: Ricercatori scoprono potenziale bersaglio per il trattamento di malattie autoimmuni).
I ricercatori Penn hanno dimostrato che la loro nuova tecnica tratta con successo la malattia autoimmune in un modello di topo, senza effetti che potrebbero danneggiare i tessuti sani.
I risultati dello studio sono stati pubblicati on line dalla prestigiosa rivista Science .
” Questa è una strategia potente per indirizzare le cellule autoimmuni risparmiando le cellule immunitarie sane che ci proteggono dalle infezioni”, ha detto il co-autore senior dello studio Aimee S. Payne, Professore Associato di Dermatologia.
Payne e il co-autore senior Michael C. Milone, MD, PhD, un assistente Professore di Patologia e Medicina, hanno preso spunto dalla strategia anti-cancro che utilizza cellule T progettate per distruggere le cellule maligne in alcune leucemie e linfomi .
“Il nostro studio apre in modo efficace l’applicazione di questa tecnologia anti-cancro al trattamento di una gamma molto più ampia di malattie, tra cui malattie autoimmuni e rigetto di trapianto d’organo”, ha spiegato Milone.
L’elemento chiave della nuova strategia si basa su un recettore target chiamato recettore chimerico dell’antigene che può essere artificialmente progettato nelle cellule T dei pazienti. Negli studi umani, i ricercatori hanno rimosso alcune cellule T dai pazienti attraverso un processo simile alla dialisi e poi le hanno ingegnerizzate in laboratorio per aggiungere ad esse il gene per esprime il nuovo recettore nelle cellule T. Le nuove cellule vengono quindi moltiplicate in laboratorio prima di essere re-infuse nel paziente. Le cellule T usano i loro recettori CAR per legarsi alle molecole sulle cellule bersaglio e l’atto di legarsi fa scattare un segnale interno che attiva con forza le T-cellule in modo che rapidamente distruggono i loro obiettivi.
Il concetto di base delle cellule T CAR è stato descritto per la prima volta alla fine del 1980, principalmente come una strategia anti-cancro, ma le sfide tecniche hanno ritardato la sua traduzione in terapie di successo.
Questa brillante idea di trasformare una cellula T in medicina “vivente” ha dato vita a cellule T CAR, la cui attività clinica è stata confermata nella leucemia linfoblastica acuta (ALL) da diverse squadre degli Stati Uniti.
CCR cellule T (cellule T per i vettori di un recettore chimerico) sono cellule T del paziente che vengono poi geneticamente modificate in vitro in modo da renderle capaci di esprimere un recettore artificiale, detto appunto, chimerico. Questo recettore è progettato in modo che la porzione extracellulare riconosce in modo specifico un antigene per evitare effetti negativi su altri organi del paziente.
Dal 2011, trattamenti sperimentali con le cellule T per leucemie e linfomi a cellule B hanno avuto successo in alcuni pazienti per i quali tutte le terapie standard avevano fallito.
Le cellule B che producono anticorpi, possono anche causare l’autoimmunità. Payne e un ricercatore post-dottorato del suo laboratorio, Christoph T. Ellebrecht, MD, hanno concentrato la loro attenzione sulla tecnologia che utilizza le cellule T autologhe come una potenziale arma contro le malattie autoimmuni. In seguito,il laboratorio di Payne ha collaborato con Milone, studioso della tecnologia che utilizza le cellule T CAR, nella speranza di trovare un nuovo modo efficace per il trattamento di questi disturbi.
“Abbiamo pensato di adattare questa tecnologia che è efficace nell’uccidere in modo specifico tutte le cellule B che producono anticorpi che causano la malattia autoimmune”, ha detto Milone.
“Il target delle sole cellule che causano l’autoimmunità è stato l’obiettivo finale della nuova terapia”, ha osservato Payne.
Un altro recettore specifico per la malattia
Nel nuovo studio, del quale Ellebrecht è stato il primo autore, il team ha preso di mira una malattia della pelle chiamata pemfigo volgare. Questa condizione si verifica quando gli anticorpi di un paziente attaccano le molecole che normalmente tengono insieme le cellule della pelle. Se non trattata, la malattia causa vasta vesciche sulla pelle ed è quasi sempre fatale, ma negli ultimi decenni la condizione viene curata con farmaci immunosoppressori come il prednisone, micofenolato mofetile e rituximab.
Per il trattamento di PV senza causare ampia immunosoppressione, il team di Penn ha progettato un recettore artificiale tipo CAR con il potenziale di indurre le cellule T dei pazienti ad attaccare solo le cellule B che producono anticorpi nocivi anti- Dsg3.
Il team ha sviluppato un “recettore chimerico” o CAAR. Il recettore artificiale reagisce come un richiamo per le cellule B che colpiscono Dsg3, portandole al contatto fatale con le cellule T terapeutiche.
Le cellule T ingegnerizzate hanno avuto successo anche in un modello murino di PV: il trattamento ha causato la morte delle cellule B specifiche per la desmogleina ed è riuscito a prevenire la formazione di vesciche e altre manifestazioni di autoimmunità negli animali.
” La desmogleina è una proteina essenziale per il reciproco ancoraggio delle cellule dell’epidermide. Le vere strutture di ancoraggio sono i desmosomi i cui più importanti costituenti sono le desmogleine. Di queste esistono diversi tipi, localizzate in modo differente nei vari strati dell’epidermide. La loro combinazione previene il distacco delle cellule tra loro interconnesse e conserva integra la cute. Una grave malattia della cute, il pemfigo, è causata dalla presenza di anticorpi anti d. che alterano i punti di contatto tra le cellule, disaggregando le une dalle altre“.
“Siamo stati in grado di dimostrare che il trattamento ha ucciso tutte le cellule B specifiche per Dsg3, una prova di concetto che questo approccio funziona”, ha detto Payne.
Le terapie con le cellule T possono essere complicate da molti fattori. Ma in questi esperimenti, le cellule ingegnerizzate create dagli degli scienziati Penn hanno mantenuto la loro potenza, nonostante la presenza di anticorpi anti-Dsg3 che brulicavano sui loro recettori artificiali. Inoltre, non ci sono stati segni che le cellule T ingegnerizzate hanno causato effetti collaterali colpendo i bersagli cellulari sbagliati nei topi.
Il team ha ora intenzione di testare il nuovo trattamento sui cani che possono anche sviluppare il pemfigo e spesso muoiono a causa della malattia.
Sono all’ orizzonte, per gli scienziati Penn, applicazioni della tecnologia delle cellule T CAAR ad altri tipi di autoimmunità. Il rigetto immunitario che complica i trapianti di organi che normalmente richiedono una terapia a base di farmaci immunosoppressori a lungo termine, può anche essere curabile con la tecnologia delle cellule T CAAR.
Fonte: Penn Medicine