Il diabete di tipo 2 è in procinto di essere ridefinito come una malattia autoimmune piuttosto che una malattia metabolica, secondo un nuovo studio pubblicato su Nature Medicine. I risultati dello studio potrebbero portare a nuovi trattamenti che colpiscono il sistema immunitario invece di cercare di controllare lo zucchero nel sangue.
Come parte dello studio i ricercatori hanno dimostrato che un anticorpo chiamato anti-CD20, che si rivolge e elimina le cellule B mature del sistema immunitario, ha bloccato il diabete di tipo 2 in via di sviluppo nei topi di laboratorio inclini a sviluppare la malattia e riportato i loro livelli di zucchero nel sangue, alla normalità.
Anti-CD20, disponibile negli Stati Uniti con i marchi Rituxan e MabThera, è già stato approvato come trattamento per alcune malattie autoimmuni e per il cancro del sangue negli esseri umani.
I ricercatori sono convinti che la resistenza all’insulina, il segno distintivo del diabete di tipo 2 (a differenza di diabete di tipo 1, dove le cellule produttrici di insulina sono distrutte), è il risultato di cellule B e di altre cellule immunitarie che attaccano i tessuti del corpo.
Daniel Winer, primo autore della ricerca e Endocrine pathologist alla University Health Network of the University of Toronto in Ontario, ha dichiarato alla stampa: “Siamo in un processo di ridefinizione del diabete di tipo 2, una delle malattie più comuni in America, come una malattia autoimmune, piuttosto che una malattia puramente metabolica.Questo lavoro cambierà anche il modo di pensare l’obesità e avrà probabilmente un forte impatto in medicina, negli anni a venire, spostando l’attenzione dei medici sui trattamenti immunomodulanti per il diabete di tipo 2 “.
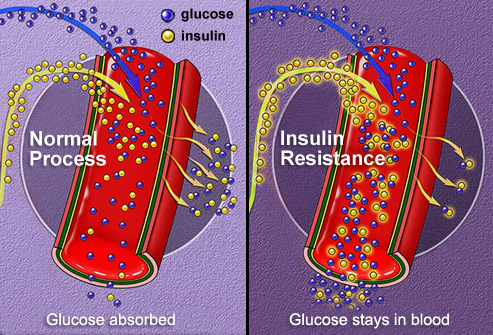
La scoperta porta il diabete di tipo 2, fino ad ora considerato una malattia metabolica, più vicino al diabete di tipo 1, dove gli attacchi del sistema immunitario distruggono le cellule che producono insulina nel pancreas. Il diabete di tipo 2 si verifica quando i tessuti del corpo gradualmente diventano sempre più resistenti all’insulina, l’ormone che permette l’ingresso del glucosio nelle cellule. Senza l’insulina, il glucosio resta in circolo aumentando sempre più il livello della glicemia e privando le cellule della loro fonte primaria di energia.
Non sappiamo che cosa porta i tessuti a diventare resistenti all’insulina nel diabete di tipo 2, ma sappiamo che è legato all’obesità. Co-primi autori dello studio insieme a Daniel Winer sono suo fratello gemello Shawn Winer dell’ Hospital for Sick Children presso l’Università di Toronto e Lei Shen, ricercatore associato dell’Università di Toronto. L’autore principale dello studio è Edgar Engleman, Direttore Stanford’s Blood Center.
Alcuni anni fa, Daniel e Shawn Winer hanno iniziato a pensare che le cellule immunitarie, comprese le cellule T (per lo più coinvolte nella risposta immunitaria cellulo-mediata) e le cellule B (coinvolte nella risposta anticorpale), possono causare infiammazione nel tessuto adiposo che circonda e protegge gli organi interni.
Alimentando i topi con una dieta con un elevato contenuto di grassi, dieta ipercalorica, si sviluppa questo tipo di infiammazione (una cosa simile accade negli esseri umani con diabete di tipo 2). Così le cellule di grasso cominciano a morire rovesciando i loro contenuti che le cellule di pulizia del sistema immunitario, i macrofagi, vanno ad assorbire.
Engleman ha detto:”Questa reazione immunitaria provoca il caos nel tessuto adiposo”.
Studiando la reazione più da vicino, i ricercatori hanno trovato che l’infiammazione coinvolge non solo i macrofagi, ma anche le cellule T e le cellule B, che gradualmente inibiscono la capacità delle restanti cellule grasse di rispondere all’insulina, causando l’afflusso e l’aumento di acidi grassi nel sangue con conseguenze come malattia del fegato grasso, colesterolo alto, pressione alta e la resistenza all’ insulina.
Per verificare le proprie idee, (un articolo del 2009 pubblicato in Nature Medicine con Shawn Winer come primo autore, ha già descritto questo lavoro) i ricercatori hanno alimentato topi di laboratorio con una dieta ad alto contenuto di grassi e con una dieta ad alto contenuto calorico, in modo che nel giro di poche settimane sono diventati obesi e la loro glicemia è aumentata. Ma quando i ricercatori hanno bloccato l’azione delle cellule T, le cellule del sistema immunitario che attivano le risposte all’interno delle cellule nel tessuto, i topi non hanno sviluppato il diabete.
Così i ricercatori hanno iniziato ad indagare le cellule B, le cellule che funzionano stimolando le cellule T per la produzione di anticorpi. Essi erano interessati alle cellule B, perché gli anticorpi non solo proteggono il corpo dalle infezioni, ma possono anche causare la malattia. Per questa parte del lavoro, il team ha geneticamente modificato i topi affinchè fossero privi delle cellule B e poi li ha nutriti con una dieta ad alto contenuto di grassi e alto contenuto di calorie. Questi topi geneticamente modificati non hanno sviluppato la resistenza all’insulina, ma quando sono stati iniettati con le cellule B o anticorpi prelevati da topi sani, la loro capacità di metabolizzare il glucosio è diminuita, i loro livelli di insulina a digiuno sono aumentati e sono diventati obesi e insulino- resistenti.
Per vedere se tale effetto si verifica negli esseri umani, i ricercatori hanno poi studiato 32 le persone in sovrappeso, abbinate per età e peso che differivano solo per la loro sensibilità all’insulina. Essi hanno scoperto che le persone con insulino-resistenza producevano gli anticorpi contro alcune delle loro proteine, cosa che non accadeva nelle persone che non erano resistenti all’insulina.
” Questi risultati sono molto suggestivi: lo sviluppo di insulino-resistenza nell’uomo coinvolge il corpo che prende di mira le proprie proteine. La sperimentazione collega davvero il concetto di insulino-resistenza all’ autoimmunità,” ha spiegato. Winer che ritiene possibile sviluppare vaccini contro il diabete di tipo 2.
Nella fase finale dello studio, i ricercatori hanno testato l’effetto di un l’anticorpo anti-CD20, chiamato Rituximab e già approvato dalla FDA, sui topi nutriti con una dieta ad alto contenuto di grassi e alto contenuto calorico, per 6 settimane.
Essi hanno dimostrato che l’anti-CD20 si attacca alle cellule B mature e le prende si mirati per distruggerle. Tuttavia, l’anti-CD20 non ha impedito la produzione di nuove cellule B dopo un primo periodo di trattamento. I topi hanno migliorato la loro capacità di metabolizzare il glucosio e i loro livelli di insulina a digiuno sono aumentati, ma dopo 40 giorni, quando il trattamento è stato interrotto, hanno cominciato a sviluppare di nuovo la resistenza all’insulina, allorchè sono state generate nuove cellule B.
I ricercatori mettono in guardia da conclusioni affrettate su come Rituximab lavorerà negli esseri umani, soprattutto se il loro diabete di tipo 2 è già stato diagnosticato.
Engleman ha spiegato: ” Anche se i nostri risultati “suggeriscono fortemente che la modulazione immunitaria deve essere considerata come una potenziale terapia umana”, fino a quando non saremo in grado di dimostrare questi effetti negli esseri umani e con successo testare terapie in studi clinici “, la dieta e l’esercizio fisico sono ancora i modi migliori per prevenire il diabete di tipo 2 negli esseri umani”.
“B cells promote insulin resistance through modulation of T cells and production of pathogenic IgG antibodies.”
Daniel A Winer, Shawn Winer, Lei Shen, Persis P Wadia, Jason Yantha, Geoffrey Paltser, Hubert Tsui, Ping Wu, Matthew G Davidson, Michael N Alonso, Hwei X Leong, Alec Glassford, Maria Caimol, Justin A Kenkel, Thomas F Tedder, Tracey McLaughlin, David B Miklos, H-Michael Dosch & Edgar G Engleman.
Nature Medicine