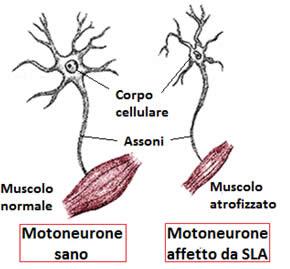
Utilizzando metodi avanzati di sequenziamento del DNA, i ricercatori hanno identificato un nuovo gene associato con la SLA, sclerosi laterale amiotrofica.
La SLA è una malattia neurodegenerativa devastante che provoca la perdita di tutti i movimenti volontari.
Il sequenziamento genetico di prossima generazione di exomes ( porzioni codificanti proteine) di 2.974 pazienti affetti da SLA e 6.405 controlli, rappresenta il più grande studio condotto fino ad oggi per il sequenziamento genetico nella condizione.
Anche se molto si sa sulle basi genetiche della SLA familiare, solo pochi geni sono stati definitivamente collegati alla SLA sporadica che rappresenta circa il 90% di tutti i casi di SLA.
Il nuovo gene associato alla malattia, chiamato TBK1, svolge un ruolo chiave nel punto di intersezione di due vie cellulari essenziali: infiammazione ( reazione a lesioni o infezioni) e autofagia ( un processo cellulare coinvolto nella rimozione di componenti cellulari danneggiuate). Lo studio che è stato condotto da un Consorzio Internazionale sulla SLA ed include scienziati e medici della Columbia University Medical Center (CUMC), Biogen Idec, e HudsonAlpha Istituto per la biotecnologia, è stato pubblicato oggi nell’edizione online di Science.

Staminali pluripotenti indotte derivate dalle cellule di neuroni motori provenienti da un paziente SLA (a sinistra) rispetto alle cellule normali (a destra). Le cellule vengono utilizzate per studiare il ruolo del TBK1 geni e OPTN nella SLA. Credit: Columbia University .
” L’identificazione di TBK1 è importante per la comprensione della patogenesi della SLA, soprattutto perchè le vie infiammatorie e autofogia sono state precedentemente già implicate nella malattia”, ha detto ha detto Lucie Bruijn, PhD, Chief Scientist per l’Associazione SLA. ” Il fatto che TBK1 rappresenta l’1% della SLA, aumenta significativamente la nostra comprensione delle basi genetiche della malttia. Questo studio, che unisce gli sforzi di più di due dozzine di laboratori in sei paesi, evidenzia anche la natura globale e collaborativo della ricarca di oggi sulla SLA. Questo studio dimostra che gli studi genetici su larga scala possono aiutarci ad individuare percorsi biologici chiave rilevanti nella SLA che poi diventeranno il fulcro per lo sviluppo di nuovi trattamenti. La SLA è una malattia incredibilmente varia, causata da decine di diverse mutazioni genetiche, che stiamo iniziando a scoprire. Più mutazioni identifichiamo, meglio possiamo decifrare e influenzare i sentieri che portano alla malattia”, ha aggiunto il co-leader David B. Goldstein, PhD, professore di genetica e direttore del nuovo Istituto per la Medicina Genomica al CUMC.
Gli altri co-leader dello studio sono Richard M. Myers, PhD, Presidente e Direttore scientifico di HudsonAlpha e Tim Harris, PhD, DSC, Senior Vice President, Tecnologia e Scienze traslazionale, Biogen Idec.
Attraverso la ricerca che ha utilizzato l’enorme database generato nello studio sulla SLA, il dottor Goldstein ed i suoi colleghi hanno scoperto diversi geni che sembrano contribuire alla malattia, in particolare TBK1 (TANK-Binding Kinase 1), che non era stato rilevato in precedenti studi su scala ridotta . Mutazioni TBK1 sono apparse in circa l’ 1% dei pazienti affetti da SLA, gran parte nel contesto di una malattia complessa con più componenti genetiche, secondo il Dr. Goldstein. Lo studio ha anche scoperto che un gene chiamato OPTN, pensato per giocare un ruolo minore nella SLA, potrebbe in realtà essere un fattore importante nello sviluppo della malattia.
“Sorprendentemente, la proteina TBK1 e optineurin, che è codificata dal gene OPTN, interagiscono fisicamente e funzionalmente. Entrambe le proteine sono necessarie per la normale funzione di vie infiammatorie e autofagia e ora abbiamo dimostrato che le mutazioni nel gene sono associate con SLA “, ha detto il dottor Goldstein. “Così non sembra esserci alcun dubbio che aberrazioni nelle vie che richiedono TBK1 e OPTN sono importanti in alcuni pazienti affetti da SLA”.
Diversi composti che influenzano la segnalazione TBK1 sono già stati sviluppati per l’uso nel cancro, in cui il gene svolge un ruolo nella sopravvivenza delle cellule tumorali.
Sembra ormai chiaro che i futuri trattamenti per la SLA non saranno ugualmente efficace per tutti i pazienti a causa della diversità genetica della malattia. In ultima analisi, saranno disponibili terapie più efficaci, in grado di utilizzare i dati genetici di ogni paziente SLA per un trattamento individualizzato.
Fonte:Exome sequencing in amyotrophic lateral sclerosis identifies risk genes and pathways. Elizabeth T. Cirulli, Richard M. Myers, David B. Goldstein et al. Science, 2015. DOI: 10.1126/science.aaa3650