Gli scienziati della UCLA hanno sviluppato un nuovo promettente metodo per trattare i tumori ginecologici. L’approccio si concentra su una proteina chiamata p53 che è comunemente mutata nelle donne affette da carcinoma ovarico sieroso, la forma più letale di cancro dell’apparato riproduttivo. In molte donne, il cancro ovarico è già molto avanzato al momento della diagnosi e quindi difficile da trattare.
La scoperta è il risultato di uno studio di tre anni co-diretto dal Dott. David Eisenberg e Sanaz Memarzadeh, membri della UCLA Jonsson Comprehensive Cancer Center. I risultati, che sono stati pubblicati online sulla rivista Cancer Cell, potrebbero in ultima analisi portare a nuove terapie mirate per molti altri tipi di cancro portatori di mutazioni di p53.
P53 è conosciuto come il “guardiano del genoma”. Esso impedisce alle cellule danneggiate di riprodursi bloccando la loro crescita fino a quando il danno non è stato riparato e nel caso in cui il danno non può essere riparato, promuove la morte cellulare.
Ma le mutazioni, che si trovano nel 96% delle pazienti con alto grado di tumori ovarici sierosi, possono causare in p53 la formazione di grumi o “aggregati” che compromettono la normale funzione della proteina. Come risultato, le cellule danneggiate possono moltiplicarsi in maniera incontrollabile, portando allo sviluppo del cancro.
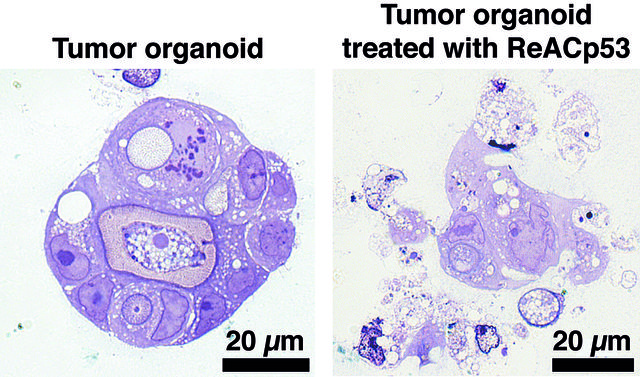
Gli scienziati UCLA hanno sviluppato e testato un peptide chiamato ReACp53, che penetra le cellule tumorali e impedisce a p53 mutato di aggregarsi. La tecnica ripristina la normale funzione di p53, causando la morte delle cellule del cancro ovarico.
“Il nostro laboratorio ha lavorato per 15 anni sugli aggregati di proteine amiloidi che causano malattie come l’Alzheimer e il morbo di Parkinson”, ha detto Eisenberg, che è anche Professore di chimica biologica e un membro della UCLA-DOE Institute. “Questi aggregati sono organizzati come fibre 500 volte più piccole rispetto alla larghezza di un capello e rappresentano una vera sfida”.
“Questo approccio è stato originariamente sviluppato per le malattie neurodegenerative e ora lo stiamo applicando alla terapia del cancro”, ha spiegato Alice Soragni, del laboratorio UCLA di Eisenberg e primo autore dello studio. “Abbiamo identificato segmenti appiccicosi che causano in p53 i grumi, utilizzando un algoritmo che ha determinato la loro struttura e quindi progettato ReACp53 per bloccare questo processo”, ha aggiunto Soragni. “Questo può impedire alla proteina l’ aggregazione in modo che possa svolgere il suo lavoro e uccidere le cellule tumorali”.
I ricercatori hanno isolato cellule tumorali da pazienti e riprodotto piccoli tumori in una piastra di Petri. I “mini-tumori” sono estremamente utili per lo sviluppo di farmaci, perché riproducono fedelmente diverse caratteristiche del tumore originale”.
“I risultati sono stati notevoli, con una significativa contrazione dei tumori”, ha detto Memarzadeh, che è anche Professore associato di ostetricia e ginecologia e Direttore del G.O. Discovery Laboratory al the Eli and Edythe Broad Center of Regenerative Medicine and Stem Cell Research.
In un modello fisiologico, l’approccio non ha prodotto evidenti effetti collaterali e ReACp53 è stato ben tollerato.
Più dell’80% delle donne con stadio avanzato di cancro ovarico ha esperienze di ricadute anche dopo ripetuti interventi chirurgici e più cicli di chemioterapia e questo nuovo approccio è efficace per curare la malattia e potrebbe essere un importante passo avanti nella prevenzione del cancro. Più di 15.000 donne ogni anno negli Stati Uniti muoiono a causa di tutti i tipi di cancro ovarico.